Loi de mélange pour la viscosité
Une loi de mélange pour la viscosité est une loi exacte ou approchée, parfois empirique, visant à prédire la viscosité dynamique d'un mélange homogène de gaz ou de liquides.
Pour les liquides
Loi de mélange d'Arrhenius
La première de ces lois de mélange, dite loi de mélange d'Arrhenius, a été publiée par Svante Arrhenius en 1887[1]. Elle postule que le logarithme de la viscosité d'un mélange de deux liquides est une combinaison linéaire des logarithmes des viscosités des espèces mélangées. Ainsi, pour deux espèces :
où :
- est la viscosité du mélange,
- la fraction molaire du produit no i ()
- la viscosité du produit no i.
La loi se généralise naturellement à un mélange impliquant un nombre N d'espèces () :
- .
Loi de mélange de Grunberg-Nissan
La théorie de Grunberg-Nissan (1949) précise la loi donnée par Arrhenius, en introduisant les termes qui modifient la viscosité et sont dus aux interactions entre deux espèces[2] :
- .
Les paramètres d’interaction n'ont pas de fondement théorique, ils sont ajustés sur les données expérimentales[3]. Ils sont en général négligeables lorsque les espèces concernées sont de nature chimique similaire[4].
Pour les gaz
La théorie cinétique des gaz permet d'obtenir rigoureusement la viscosité d'un mélange gazeux comme la solution d'un système linéaire[5],[6]. Celle-ci peut être écrite comme le quotient de deux matrices. Les solutions approchées sont alors recherchées à partir de développements limités[7],[8]. Le fait que les matrices soient à diagonale dominante permet diverses approximations de celles-ci[9].
On utilise ci-dessous les fractions molaires , les viscosités , la pression , la température , les masses molaires , les coefficients de diffusion binaires et un coefficient lié aux intégrales de collision
qui caractérise les interactions entre molécules. Lorsque l'on utilise un potentiel Lennard-Jones, on a [6].
- La première approximation a été obtenue par Buddenberg et Wilke[10] en négligeant tous les termes extra-diagonaux.
- avec
- Le coefficient qui vaut 2 est dans les faits modifié pour coller au mieux aux résultats. Dans les mélanges gazeux choisis par les auteurs de l'approximation la valeur retenue est . Pour l'air on obtient une meilleure précision en prenant [8].
- Brokaw propose un calcul approché des termes extra-diagonaux[11] qui permet d'identifier , de l'ordre de 1,3
- Wilke a proposé une simplification[12] permettant de n'utiliser que le coefficients d'auto-diffusion à partir d'un potentiel sphères dures et en supposant tous les égaux entre eux.
- En fait on montre[8] que le recours à un potentiel simple n'est pas nécessaire et que l'on peut écrire
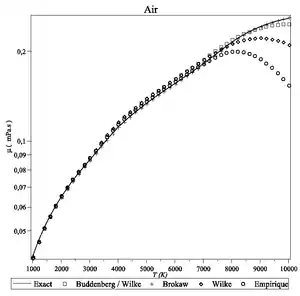
Il existe d'autres approximations plus complexes et plus précises[9],[8] mais il faut noter qu'une simple loi de mélange , bien que sans justification théorique, donne des résultats très honorables (voir courbe). Dans cette expression, est la fraction massique.
Notes et références
- (de) Svante Arrhenius, « Über die Innere Reibung Verdünnter Wässeriger Lösungen », Zeitschrift für Physikalische Chemie, vol. 1, no 1, , p. 285-298 (DOI 10.1515/zpch-1887-0133).
- (en) L. Grunberg et Alfred H. Nissan, « Mixture Law for Viscosity », Nature, vol. 164, no 4175, , p. 799–800 (ISSN 1476-4687, DOI 10.1038/164799b0, lire en ligne, consulté le ).
- (en) Hamid Reza Rafiee, Shahram Ranjbar et Fariborz Poursalman, « Densities and viscosities of binary and ternary mixtures of cyclohexanone, 1,4-dioxane and isooctane from T=(288.15 to 313.15)K », The Journal of Chemical Thermodynamics, vol. 54, , p. 266–271 (DOI 10.1016/j.jct.2012.05.005, lire en ligne, consulté le ).
- (en) Pedro Benjumea, John Agudelo et Andrés Agudelo, « Basic properties of palm oil biodiesel–diesel blends », Fuel, vol. 87, no 10, , p. 2069–2075 (ISSN 0016-2361, DOI 10.1016/j.fuel.2007.11.004, lire en ligne, consulté le ).
- (en) Sydney Chapman et Thomas George Cowling, The Mathematical Theory of Non-uniform Gases : an account of the kinetic theory of viscosity, thermal conduction, and diffusion in gases, Cambridge/New York/Port Chester etc., Cambridge University Press, , 422 p. (ISBN 0-521-40844-X)
- (en) Joseph Oakland Hirschfelder, Charles Francis Curtiss et Robert Byron Bird, Molecular Theory of Gases and Liquids, John Wiley and Sons, (ISBN 978-0-471-40065-3)
- (en) J. H. Ferziger et H. G. Kaper, Mathematical Theory of Transport Processes in Gases, North Holland Publishing,
- (en) Duffa G., Ablative Thermal Protection Systems Modeling, Reston, VA, AIAA Educational Series, , 431 p. (ISBN 978-1-62410-171-7)
- (en) Yeram Sarkis Touloukian, S. C. Saxena et P. Hestermans, Viscosity, vol. 11, IFI/Plenum Press, (ISBN 0-306-67031-3, lire en ligne)
- (en) J. W. Buddenberg et C. R. Wilke, « Calculation of Gas Mixture Viscosities », Industrial Engineering & Chemistry, vol. 41, no 7, , p. 1345-1347 (DOI 10.1021/ie50475a011)
- (en) R. S. Brokaw, « Approximate Formulas for the Viscosity and Thermal Conductivity of Gas Mixtures », Journal of Chemical Physics, vol. 29, no 2, , p. 391-397 (DOI 10.1063/1.1744491)
- (en) C. R. Wilke, « A Viscosity Equation for Gas Mixtures », Journal of Chemical Physics, vol. 18, no 4, , p. 517-519 (DOI 10.1063/1.1747673)
- Portail de la physique
- Portail des sciences des matériaux