Interaction agostique
Le mot agostique a été introduit par Malcom Green et Maurice Brookhart dans le domaine de la chimie organométallique pour décrire une interaction liante faible entre un métal de transition et un lien C–H lié à un atome de carbone qui est tenu près du métal central par le biais d'une interaction π ou σ[1].
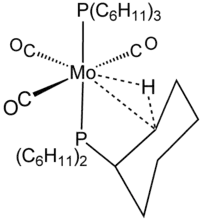
Le mot provient du grec pour « tenir près de soi ». Cette interaction ressemble de près à l'état de transition d'une addition oxydante ou d'une élimination réductrice. Les interactions agostiques sont le mieux démontrées en cristallographie mais peuvent être déduites de la présence d'un pic RMN 1H qui est décalé vers les champs forts comparé à celui d'un aryle ou alcane normal, se rapprochant de celui d'un ligand hydrure. La constante de couplage JCH est généralement abaissée à 70–100 Hz au lieu des 125 Hz normalement attendus pour une liaison hydrogène–carbone sp³. L'énergie de l'interaction est estimée à environ 10–15 kcal·mol-1 (40–60 kJ·mol-1) à partir de résultats expérimentaux d'études de chimie numérique. Cette interaction est donc légèrement plus forte que la plupart des liaisons hydrogène.
Les liens agostiques jouent parfois un rôle dans les réactions catalytiques en augmentant la « rigidité » des états de transition. Par exemple, dans une catalyse Ziegler-Natta, le centre métallique, fortement électrophile, a des interactions agostiques avec la chaîne de polymère en formation.
Le terme agostique a été étendu de manière impropre afin d'inclure d'autres interactions liantes à trois centres comme la complexation de H2 sur le tungstène illustrée par W(CO)3(PiPr3)2H2[2].
Références
- (en) Maurice Brookhart et Malcolm L.H. Green, « Carbon—hydrogen-transition metal bonds », Journal of Organometallic Chemistry, vol. 250, no 1, , p. 395-408 (DOI 10.1016/0022-328X(83)85065-7)
- Gregory J. Kubas, Metal Dihydrogen and σ-Bond Complexes : Structure, Theory, and Reactivity, Springer, , 472 p. (ISBN 978-0-306-46465-2, lire en ligne)
Lien externe
- (en) Liaison agostique
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Agostic interaction » (voir la liste des auteurs).
- Portail de la chimie