Cryptand
Les cryptands sont une famille de ligands synthétiques bicycliques ou polycycliques pour une sorte de cation. En 1987, le prix Nobel de chimie a été attribué à Donald J. Cram, Jean-Marie Lehn, et Charles J. Pedersen pour leur travail sur les utilisations des cryptands et les éthers couronnes, ce qui a donné naissance au domaine de la chimie supramoléculaire.
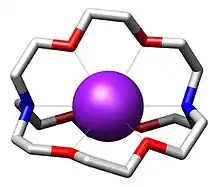
Le terme cryptand évoque étymologiquement que le ligand lie les substrats ou ses molécules-cibles dans une crypte, c'est-à-dire de manière durable, comme on conservait les morts dans une tombe dans une crypte.
Ces molécules sont des équivalents tridimensionnels des éthers-couronnes, mais ils sont plus sélectifs et « complexent » plus fortement l'ion réactif.
Structure
Le cryptand le plus courant est le N≡[CH2CH2-O-CH2CH2-O-CH2CH2]3≡N, dont la formule IUPAC est le 1,10-diazote-4,7,13,16,21,24-hexaoxo-bicyclo[8.8.8]hexacosane (dans cette nomenclature, la numérotation des noyaux commence par un des atomes d'azote et suit en zigzag chaque oxygène ou carbone le long de chacune des trois branches, en numérotant deux fois chaque azote et terminant par le second azote, mais on ne conserve pour eux que le plus petit numéro ; la numération implicite des atomes de carbone n'a pas besoin d'être précisée, on précise seulement la place des atomes d'oxygène).
Toutefois cette nomenclature « bicyclo » traduit mal que, dans la conformation tridimensionnelle du complexe, les deux cycles formés par les 3 ponts hexacosanes (reliés à leurs extrémité par les amines communs), vont en fait se « replier » et s'associer pour former un troisième cycle équivalent autour d'un espace central, ces 3 cycles associés étant plus stables que les deux cycles d'une simple structure plane (aucune paire de ponts n'est « privilégiée » par rapport aux deux autres paires possibles : chacun des ponts a les mêmes propriétés électrochimiques, le repliement se produit naturellement sous le seul effet des vibrations thermiques et forme alors un équilibre stable dans sa conformation sphérique). De nombreuses structures moléculaires à double cycle ne peuvent se replier pas de cette façon stable qu'en cas de symétrie des branches de leurs cycles, cette symétrie étant facilement brisée en cas d'interaction avec un pôle de l'une d'elles.
À proximité toutefois d'un cation, une paire de ponts du complexe peut interagir par la polarité de ses fonctions éthers : ces ponts peuvent alors facilement « s'écarter » et le cation s'il est assez petit est alors dirigé vers l'intérieur du complexe où il va ensuite se lier de façon également équivalente aux fonctions éther du troisième pont ; le complexe se referme à nouveau dans sa structure à 3 cycles liés « emprisonnant » le cation fortement monopolaire dans une nouvelle structure hexapolaire, dont chacun des pôles est beaucoup plus faible.
Ce composé est appelé cryptand[2,2,2], où les chiffres indiquent le nombre de fonctions éthers dans chacun des trois « ponts » liant les « capsules » d'azote amine. Beaucoup de cryptands sont commercialisés sous la marque « Kryptofix ».
Utilisations

Bien qu'ils soient coûteux et plus difficiles à préparer, les cryptands offrent une meilleure sélectivité et force de liaison que d'autres complexants pour les métaux alcalins, comme les éther-couronnes. Ils permettent d'augmenter la solubilité des sels dans certains solvants, en accroissant la réactivité des anions du cristal. Par exemple, le sulfate de baryum est 10 000 fois plus soluble dans l'eau en présence du cryptand [2,2,2]. Ils peuvent également être utilisés comme catalyseur de transfert de phase.
Molécules dérivées
Avec le développement de la chimie supramoléculaire, de nombreux dérivés des cryptands ont été élaborés tels que les sepulchrates[2], équivalents azotés et les cryptophanes[3], cages inspirées des cyclophanes.
 Sépulchrate complexant Co3+
Sépulchrate complexant Co3+ Diastéréoisomères de cryptophane
Diastéréoisomères de cryptophane
Références
- Alberto, R.; Ortner, K.; Wheatley, N.; Schibli, R.; Schubiger, A. P.; Synthesis and properties of boranocarbonate: a convenient in situ CO source for the aqueous preparation of [99mTc(OH2)3(CO)3]+; J. Am. Chem. Soc., 2001, Vol 121, p. 3135–3136 ; doi = 10.1021/ja003932b
- I. I. Creaser, J. M. Harrowfield, A. J. Herlt, A. M. Sargeson, J. Springborg, R. J. Geue, and M. R. Snow, Journal of the American Chemical Society, 1977, 99 (9), 3181-3182
- Jacqueline Gabard and André Collet, J. Chem. Soc., Chem. Commun., 1981, 1137-1139